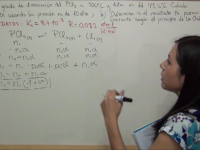Índice general de Equilibrio Químico: teoría y ejercicios
-

Equilibrio Químico Ejercicio 9: Calcular Kc con la concentración inicial y el grado de disociación
Ejercicio de calcular la constante de equilibrio Kc a partir de la concentración inicial y el grado de disociación, alfa. Ver video -

Equilibrio Químico 7.2. Principio de Le Châtelier: modificación de la presión y el volumen
La modificación de la presión y del volumen en un equilibrio químico lo altera, de forma que el sistema debe evolucionar para recuperarlo. Ver video -

Equilibrio Químico 7.3. Variación de la temperatura de un equilibrio químico: ecuación de Van't Hoff
La ecuación de Van't Hoff nos indica cómo varía la constante de un equilibrio químico al variar la temperatura, y cómo afecta esto al equilibrio. Ver video -
Reacciones de precipitación. Solubilidad y producto de solubilidad.
En las reacciones de precipitación o equilibrios de solubilidad, tenemos algunos conceptos de gran importancia, como la solubilidad y el producto de solubilidad. Ver video -

Solubilidad ejercicio 4: Determinar si se formará precipitado de BaSO4. Efecto ion común.
En este ejercicio debemos deducir si se va a formar un precipitado al mezclar una disolución de ácido sulfúrico con otra de cloruro de bario. Ver video -

Solubilidad ejercicio 5: Producto de solubilidad del AgBr y efecto ion común
Determinar cómo cambia la solubilidad del bromuro de plata cuando se adiciona bromuro de potasio, lo cual hace que se produzca el efecto ion común. Ver video -

Solubilidad ejercicio 6: solubilidad y producto de solubilidad a partir del pH. Neutralización ácido base.
En este ejercicio de selectividad calculamos la solubilidad y el producto de solubilidad de una disolución saturada a partir de su pH. Ver video -

Equilibrio Químico Ejercicio 8: Calcular la cantidad inicial de un reactivo dada Kc. Esterificación.
En la reacción de esterificación calcularemos qué cantidad inicial de etanol se requiere para obtener en el equilibrio 166 gramos de etanoato de etilo. Ver video -

Equilibrio de solubilidad: efecto del ion común y efecto salino
Cuando se tiene un equilibrio de solubilidad y se agrega otra sal, puede producir el efecto del ion común (disminuye la solubilidad) o el efecto salino. Ver video