Contenido del Vídeo
En este vídeo resolvemos un ejercicio de la PAU (Prueba de Acceso a la Universidad, Selectividad) de la comunidad autónoma de Madrid. En concreto, se trata de la pregunta 4 de la opción A, un ejercicio de termoquímica. En él debemos formular y ajustar la reacción de combustión del propano, calcular la entalpía de combustión a partir de las energías de los distintos enlaces que intervienen en la reacción (energía de los enlaces rotos menos energía de los enlaces formados) y finalmente determinar el volumen de dióxido de carbono que se producirá en el proceso, dadas ciertas condiciones. El enunciado completo es:
El propano es uno de los combustibles fósiles más utilizados.
a) Formule y ajuste su reacción de combustión.
b) Calcule la entalpía estándar de combustión e indique si el proceso es exotérmico o endotérmico.
c) Calcule los litros de dióxido de carbono que se obtienen, medidos a 25 ºC y 760 mm de Hg, si la energía intercambiada en el proceso es de 5990 kJ.
Como veremos en la explicación, la reacción de combustión del propano será:
En cuanto al segundo apartado, la fórmula que aplicaremos para el cálculo será la siguiente:
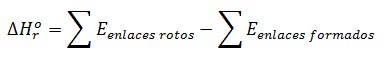
La base teórica para la realización de este ejercicio la puedes encontrar aquí:
Termodinámica teoría 13: cálculo de la entalpía de reacción a partir de las entalpías de enlace
Asimismo, a continuación puedes encontrar otros ejercicios resueltos del mismo tipo:
Ejercicio 25 Termodinámica: Entalpía de adición de halógenos a eteno y etino por entalpías de enlace
Category: Ejercicios de Termoquímica y Ejercicios Selectividad.
Etiquetas: Química Selectividad Madrid.





 Estructura Atómica
Estructura Atómica Enlace Químico
Enlace Químico Termodinámica química
Termodinámica química Equilibrio Químico
Equilibrio Químico Ácido Base
Ácido Base Redox
Redox Selectividad
Selectividad