Metales alcalinos (I): el litio
Escrito por Quimitube el 6 agosto
El litio es el más ligero de los metales (y el más ligero de los metales alcalinos, grupo 1 de la tabla periódica) y uno de los átomos más ligeros de toda la tabla periódica: solo el hidrógeno y el helio lo son más, ya que el número atómico del litio es 3. Presenta, por tanto, 3 protones en su núcleo y, si se trata de un átomo neutro, también 3 electrones en su corteza. Su configuración electrónica es 1s2 2s1; como corresponde a un metal alcalino, su última capa presenta un único electrón en un orbital de tipo s. Cuando un átomo de litio pierde dicho electrón se forma el catión litio, Li+.
Li → Li+ + 1e–
El litio es el metal más ligero de los metales alcalinos, correspondientes al grupo 1 de la tabla periódica. Todos ellos tienen un único electrón en su última capa, situado en un orbital s.
Es el metal más ligero, con una densidad que es prácticamente la mitad de la del agua, concretamente 535 kg/m3, y tiene un color plateado claro cuando no está oxidado en su superficie, en cuyo caso se ve negruzco por el proceso siguiente:
4Li(s) + O2(g) → 2Li2O(s)
Se oxida con bastante facilidad y reacciona violentamente con el agua. Esto se debe a que pierde electrones con facilidad porque su energía de ionización es pequeña, aunque es la más elevada de todos los metales alcalinos, que son las siguientes:
Energía de ionización del Litio: 513 kJ/mol
Energía de ionización del Sodio: 496 kJ/mol
Energía de ionización del Potasio: 419 kJ/mol
Energía de ionización del Rubidio: 403 kJ/mol
Energía de ionización del Cesio: 376 kJ/mol
Por este motivo, por su gran reactividad, se suele guardar conservado en aceites minerales como se ve en esta imagen:

Litio metálico flotando en un aceite mineral inerte. Se puede apreciar su color plateado claro, es precioso, ¿verdad?
Su estructura es cúbica centrada en el cuerpo:
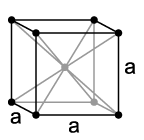
La estructura cúbica centrada en el cuerpo para el litio tiene un valor de a de 351 pm.
No se encuentra libre en la naturaleza (es decir, como litio metálico) sino combinado por su gran reactividad, aunque se puede lograr aislar y obtener el litio sólido que vemos en la imagen previa mediante electrólisis de otros compuestos de litio, esencialmente óxido de litio, Li2O o también cloruro de litio, LiCl. En este último caso, la electrolisis del cloruro de litio, se lleva a cabo fundiendo el mismo con cloruro potásico a elevada temperatura, en torno a 430ºC, siendo estas las semirreacciones que se producen para dar lugar a Li:
Cátodo: Li+(l) + e– → Li(l)
Ánodo: Cl–(l) → 1/2Cl2 (g) + e–
Vemos que en la reacción aparece el litio líquido. El motivo es que el punto de fusión del metal es de 181ºC, por lo que a la temperatura a la que se lleva a cabo la electrolisis está fundido.
A continuación podéis ver un vídeo de Periodic Table of Videos en el que se observa la reacción química entre el litio metálico y el agua. Es tan energética que incluso se forman llamas:
Esta es la reacción química que se produce cuando el litio reacciona con el agua, desprendiendo hidrógeno (un gas muy inflamable):
2 Li(s) + 2 H2O → 2LiOH (aq) + H2(g)
Si bien el litio y sus compuestos tienen múltiples aplicaciones (como medicación para determinados problemas psicológicos, como desecantes, como lubricantes, como agente en la síntesis de determinados compuestos orgánicos o como componente en aleaciones aeronáuticas) la aplicación que probablemente os resulte más conocida es como componente en las baterías ion-litio. Tanto es así, que el aumento en la producción mundial de litio desde el año 2008 ha sufrido un incremento auténticamente espectacular, por el desarrollo de las nuevas tecnologías (móviles, tablets, portátiles cada vez más ligeros…) y de materiales especiales, como cerámicas de gran ligereza. Aquí vemos una representación que lo ilustra en toneladas por año:
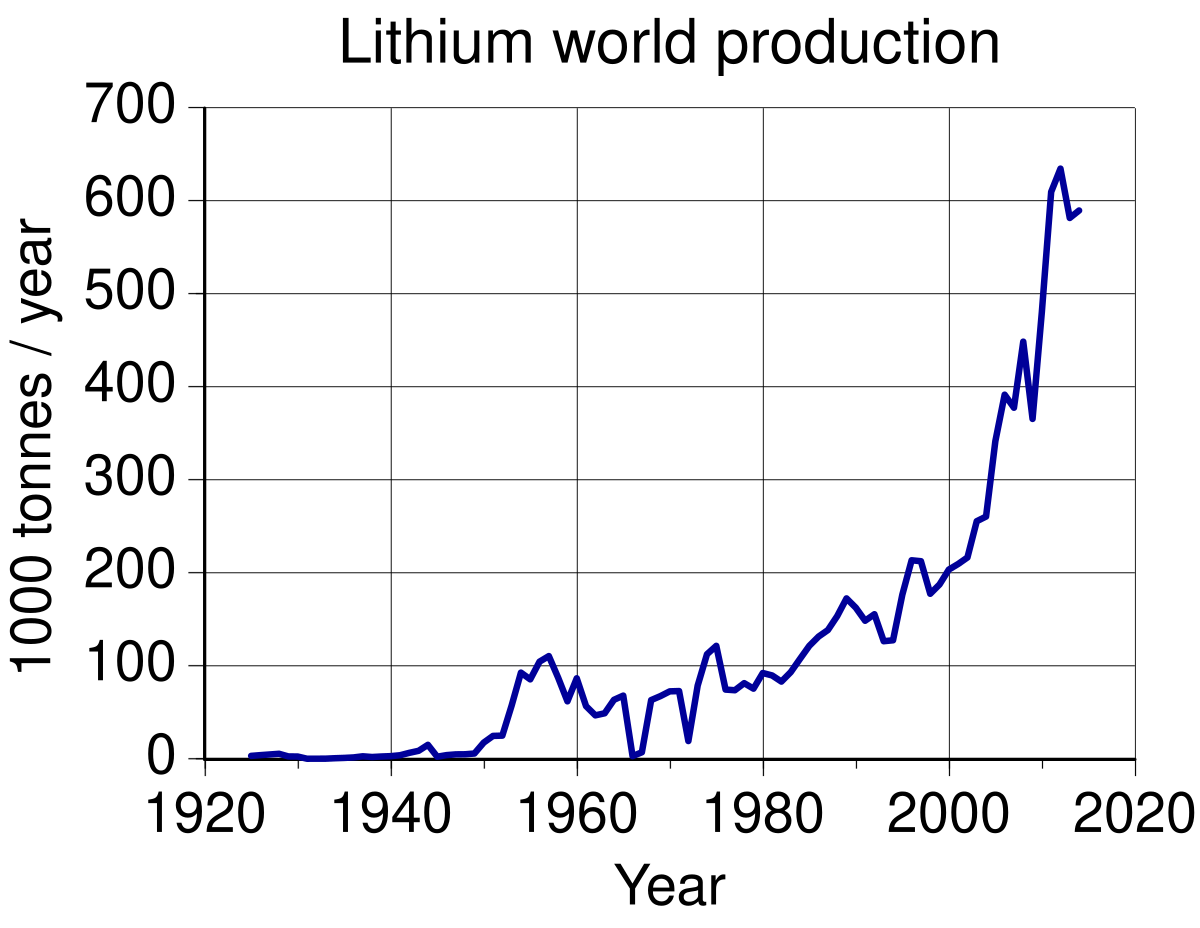
«Lithium world production» by Con-struct – U.S. Geological Survey. Licensed under CC BY-SA 3.0 via Wikimedia Commons.
En una entrada posterior hablaremos en profundidad de las baterías ion-litio y de otras alternativas que se están investigando en la actualidad basadas en el aluminio.