El fosfuro de aluminio y su letal reacción con agua para dar fosfano
Escrito por Quimitube el 5 febrero
Hace unos días se hizo público el informe forense acerca de la muerte de tres miembros de una misma familia en Sevilla en el mes de diciembre. Aunque en un principio se había sospechado que la causa del fallecimiento podía ser de origen alimentario, la gravedad del estado y la velocidad de la muerte de estas tres personas, que presentaban náuseas y vómitos severos, hizo que las pesquisas derivasen la investigación hacia una intoxicación por inhalación de algún compuesto. Trágicamente así fue: el informe concluye que sufrieron una intoxicación con fosfano, el hidruro de fósforo de fórmula PH3 (también conocido con el nombre tradicional, ya no aceptado, de fosfina). Esta es su geometría molecular:
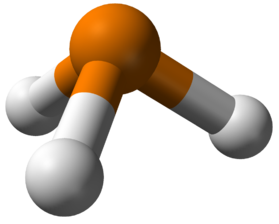
El fosfano es un gas incoloro e inflamable, con poca solubilidad en agua y de olor desagradable (similar al de algunos compuestos de azufre, como el olor de los huevos podridos o el ajo, aunque el fosfano puro es inodoro, es la presencia de fosfinas sustituidas lo que hace que huela). Se trata de un compuesto con un poder reductor muy considerable, que reacciona con el oxígeno para producir ácido fosfórico; es de esta reactividad como reductor de donde procede su potencial letal para el organismo. Si observamos su símbolo de peligrosidad vemos lo siguiente:
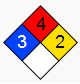
El 4 representa la inflamabilidad (sobre una escala de 4) y el 3 la peligrosidad para la salud humana. Los primeros síntomas de exposición aguda a la fosfina incluyen dolor abdominal, náuseas y vómitos, síntomas todos ellos tan habituales que hacen difícil (si no imposible, ya que se metaboliza rápidamente y no es detectable) diagnosticar una intoxicación con esta sustancia que actúa a semejante velocidad, en cuestión de horas. La exposición a niveles más altos puede producir debilidad, bronquitis y edema pulmonar hasta que finalmente lleva al fallecimiento del paciente, como así fue en este caso.
¿Y de dónde procedía el fosfano que inhaló esta familia? Procedía de la descomposición del fosfuro de alumino, AlP, sustancia utilizada como insecticida y roenticida potente precisamente por su capacidad para liberar fosfano en presencia de humedad, que se suele vender en pastillas sólidas, cubiertas de parafina y mezcladas con carbonato amónico, o en forma de polvo. Generalmente es un polvo de color gris, verde o amarillo debido a la presencia de impurezas. Esta es su estructura:
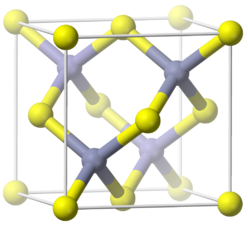
Reacciona con el agua para formar fosfano según la siguiente reacción química:
AlP (s) + 3H2O (l) → Al (OH)3 (s) + PH3 (g)
Esta reacción del fosfuro de aluminio con agua para dar fosfano es una reacción exotérmica (-166 kJ/mol). Asimismo, podemos deducir que aumentará su entropía, porque pasamos de un sólido y un líquido a un sólido y un gas; la formación de un gas provocará que la variación de entropía de la reacción, ΔS, sea positiva, por lo que su energía libre de Gibbs será negativa y la reacción será espontánea a temperatura ambiente:
ΔG = ΔH – T·ΔS < 0
Así, si el fosfuro de aluminio entra en contacto con agua, desprende PH3, y esto es lo que el informe concluye que sucedió, que los restos del sólido que había en algunos tapones de los recipientes que lo contuvieron, almacenados en un saco dentro del domicilio, entraron en contacto con agua o con la humedad ambiente y formaron el gas letal. Triste explicación la de esta entrada que nos muestra que se deben manejar con precaución algunas sustancias peligrosas y demasiado cotidianas. Es importante deshacerse de los residuos de la forma establecida, para que no puedan llegar al alcance de nadie y causar tragedias como esta.
Más información:
La familia de Alcalá de Guadaría murió tras inhalar fosfina de unos tapones





Información Bitacoras.com…
Valora en Bitacoras.com: Hace unos días se hizo público el informe forense acerca de la muerte de tres miembros de una misma familia en Sevilla en el mes de diciembre. Aunque en un principio se había sospechado que la causa del fallecimiento podía se…..
Bitacoras.com, 11 Años Antes
A VER SI PUEDEN APOYARME CON ESTA PREGUNTA. SEGUN LA REACCION QUIMICA AlP (s) + 3H2O (l) → Al (OH)3 (s) + PH3 (g) es una reacción exotérmica (-166 kJ/mol).
CUANTAS KCALORIAS SE DESPENDENDEN AL REACIONAR UN KILOGRANO DE AlP EN AGUA.
MUCHAS GRACIAS POR SU APORTE.
JAVIER DELGADO, 10 Años Antes
Hola Javier, basta que hagas cálculos estequiométricos pasando 1 kg de AlP a moles, y después sabes que 1 mol desprende 166kJ (de su entalpía). Un saludo.
QuimiTube, 10 Años Antes