¿Atracones navideños? Una ayudita química para la acidez estomacal
Escrito por Quimitube el 3 enero
– ¿Un trocito de turrón? -sugiere tu madre.
– No, gracias.
– ¿Y un polvorón?
Todo el mundo ha tomado ya aperitivo, primero, segundo, postre y café, pero el turrón y los bombones siguen apareciendo en la mesa como por arte de magia.

A éste no pude negarme
De modo que te niegas (de nuevo) educadamente:
-No, mamá, gracias, no me cabe nada más. -Y es literal. Tienes que negarte al menos 3 o 4 veces más para que, al fin, deje de insistir.
Pero… ¿la comida no era para sobrevivir? ¿Desde cuándo nos sobrealimentamos? En estas fechas navideñas, en las que los atracones se suceden uno tras otro sin freno, como cantos rodados cayendo por la ladera de una montaña, a menudo empezamos a sentir como si el esófago y el estómago nos estuvieran quemando. Y, en efecto, eso también puede ser literal: el exceso de ácido en el estómago, o la regurgitación de ácido hacia el esófago, provocan una sensación de ardor o acidez verdaderamente molesta.
Cuando ingerimos comida, ésta llega al estómago y se mezcla íntimamente con los jugos gástricos, una disolución de ácido clorhídrico (al 1% aproximadamente, lo que le confiere un pH en torno a 0,8), sales (como cloruro sódico, NaCl, y cloruro potásico, KCl) y enzimas digestivas en forma inactiva, principalmente pepsinógeno, que es el precursor de la pepsina. Los jugos gástricos son segregados por las numerosas glándulas parietales microscópicas diseminadas por la mucosa estomacal, gracias a la acción de una hormona, la gastrina, que se activa cuando llega comida al estómago.
El ácido clorhídrico segregado en el estómago posibilita que el pepsinógeno inactivo se hidrolice, desprendiéndose de algunos aminoácidos para formar la pepsina, forma activa de la enzima. La pepsina es una enzima capaz de hidrolizar proteínas (es decir, de romper enlaces peptídicos). En concreto, la pepsina únicamente rompe los enlaces peptídicos formados entre fenilalanina y fenilalanina y entre fenilalanina y tirosina.
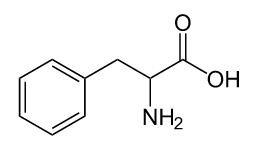
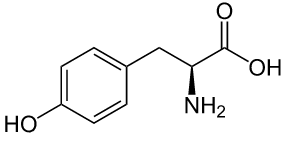
Así, las proteínas que ingresan al estómago se convierten en péptidos (cortas cadenas formadas por unos cuantos aminoácidos) o aminoácidos individuales, en función de la secuencia de la proteína ingerida. La pepsina es una enzima especial, ya que es más activa a un pH de entre 2 y 3, que es el valor de pH que toma el estómago tras la ingestión de alimentos. Por encima de pH 5 se inactiva, mientras que la mayoría de enzimas lo hacen a pH ácido. La digestión, por tanto, requiere necesariamente una concentración considerable de protones, H+, en el estómago.
Sin embargo, a veces, cuando comemos en exceso o ingerimos alimentos muy pesados (tomate, cafeína, alcohol, cítricos…), los niveles ácidos del estómago se desbaratan. Claro que lo ideal es evitar que esto suceda, pero cuando el mal ya está hecho podemos recurrir a un antiácido, útil de forma puntual (los enfermos estomacales crónicos que padecen reflujo gastroesofágico necesitan otra medicación más efectiva). Un antiácido es simplemente una base que reacciona con el exceso de ácido del estómago, neutralizándolo; por tanto, un antiácido logra aumenta el pH del estómago. Los antiácidos de neutralización directa más habituales son: bicarbonato sódico (Alka-Seltzer®), carbonato alumínico, carbonato cálcico, hidróxido de magnesio, hidróxido de aluminio o hidrotalcita.
La reacción general de neutralización del ácido estomacal con un antiácido se puede expresar como:
HCl (ácido gástrico) + Antiácido (base débil) → H2O + (CO2) + sales
Indicamos el CO2 entre paréntesis porque su producción depende del antiácido que estemos utilizando; en concreto, se generará dióxido de carbono si usamos bicarbonato o carbonato, lo cual provocará desagradables eructos (¡vaya por Dios!), tal y como se puede observar en las reacciones de neutralización correspondientes para cada uno de ellos:
NaHCO3 + HCl → NaCl + CO2 + H2O
CaCO3 + 2 HCl —> CaCl2 + CO2 + H2O
Existen otros antiácidos no producen CO2, como se puede ver en la reacción del hidróxido de aluminio y la del hidróxido de magnesio con el ácido clorhídrico:
3 HCl + Al (OH)3 → AlCl3 + 3 H2O
Mg(OH)2 + 2 HCl —> MgCl2 + 2 H2O
Sin embargo, aunque estos otros antiácidos no producen CO2, no son el carbonato y el bicarbonato los únicos con efectos secundarios. Los productos de neutralización al usar sales de calcio o de aluminio provocan estreñimiento, y las de magnesio, por el contrario, tienen efectos laxantes. Por ello, otro antiácido común es la combinación del hidróxido de aluminio y de magnesio, que contrarresta en parte estos efectos contrapuestos; es el llamado almagato, famoso por su nombre comercial, Almax®, de fórmula CH11AlMg3O12.
Mi consejo, obviamente, es intentar controlarse con las comidas navideñas pero, por si acaso, nunca está de más tener a mano algún sobrecito de antiácido para que nos ayuden a pasar mejor el trance.





Información Bitacoras.com…
Valora en Bitacoras.com: – ¿Un trocito de turrón? -sugiere tu madre. – No, gracias. – ¿Y un polvorón? Todo el mundo ha tomado ya aperitivo, primero, segundo, postre y café, pero el turrón y los bombones siguen apareciendo en la mesa como por arte de …..
Bitacoras.com, 12 Años Antes
Me encanta esta página, hay un montón de artículos interesantes, comprensibles y bien redactados
Fran, 12 Años Antes
Gracias Fran, me alegro de que te gusten, lo cierto es que le damos mucha importancia a la redacción del texto e intentamos que sea, en efecto, comprensible y entretenido. Un saludo.
QuimiTube, 12 Años Antes