Contenido del Vídeo
El enlace metálico es muy distinto a los dos tipos de enlaces que hemos visto hasta ahora: el enlace covalente y el enlace iónico. En los compuestos metálicos los átomos están muy próximos los unos a los otros y forman estructuras compactas. Además, presentan unas características propias, entre las que destaca la elevada conductividad eléctrica. Esta propiedad, la de la conductividad, requiere para ser explicada que los electrones implicados en el enlace metálico tengan libertad y facilidad de movimiento. Es por este motivo que, para que los metales tengan electrones móviles, requieren 2 características a nivel atómico: la primera, una energía de ionización baja (recordemos que la energía de ionización es la energía necesaria para arrancar un electrón de la capa de valencia) y la segunda, que posean orbitales de valencia vacíos y accesibles que permitan a los electrones moverse con facilidad.
Cualquier teoría sobre el enlace metálico debe dar explicación a esta libertad de movimiento electrónico y a las restantes propiedades de los metales. Estas son dos: la llamada teoría del gas electrónico o del mar de electrones y la teoría de bandas.
TEORÍA DEL GAS ELECTRÓNICO PARA EL ENLACE METÁLICO
En la teoría del gas electrónico (también llamada del mar de electrones o de la nube electrónica), los átomos metálicos pierden sus electrones de valencia y forman una red compacta de cationes. Por ejemplo, en el caso del sodio, cuya configuración electrónica es:
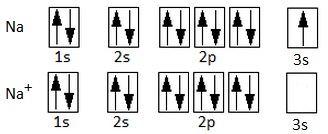
Los cationes Na+, formados por los núcleos atómicos y los electrones de las capas internas, se empaquetan y los electrones de valencia se mueven con libertad. Estos electrones no pertenecen ya a los átomos individuales, sino que son comunes a todos los átomos que forman la red. Se dice que los electrones están deslocalizados.
Dependiendo del número de electrones de valencia que tenga el metal, habrá tantos electrones deslocalizados como átomos o más. Por ejemplo, en el sodio, que pierde un electrón, habrá tantos electrones como átomos de sodio, pero en el magnesio, que tiene 2 electrones de valencia y los pierde ambos, habrá el doble de electrones que de núcleos de Mg(2+).
Así, los cationes se disponen formando un retículo cristalino compacto o empaquetamiento metálico y cada catión se rodea del número máximo de cationes vecinos. Los electrones de valencia se mueven libremente por los intersticios de la red, formando el gas electrónico y actuando, además, como un colchón que evita la repulsión entre los distintos cationes.
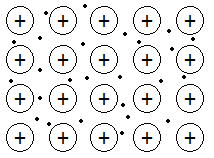
Dada la libertad de movimiento de los electrones de valencia, esta teoría para el enlace metálico explica muy bien muchas de las propiedades metálicas, tales como la elevada conductividad eléctrica y térmica. También explica la ductilidad y la maleabilidad o la resistencia a la deformación, porque las capas de cationes pueden deslizarse unas sobre las otras, manteniendo el tipo de estructura y la fortaleza del enlace.
Category: Enlace Químico y Teoría de Enlace Químico.
Etiquetas: Enlace metálico.





 Estructura Atómica
Estructura Atómica Enlace Químico
Enlace Químico Termodinámica química
Termodinámica química Equilibrio Químico
Equilibrio Químico Ácido Base
Ácido Base Redox
Redox Selectividad
Selectividad
hola!
Tengo un problema con un ejercio de calulo de volumenes, me pueden ayudar.
Dice el problema:
2CO + O2 formandose 2CO2
Determinar el volumen de aire, en CN, necesario para la combustion total de 100 litros de CO a 3atm y 27C (el aire contiene un 20% en volumen de oxigeno)
No entiendo 🙁 🙁
darliens, 12 Años Antes
Este ya lo miramos por facebook, ¿verdad? ¿Qué tal lo llevas? ¿Te salió por completo? Un saludo 🙂
QuimiTube, 12 Años Antes
ah otra cosita de la siguiente ecuacion:
Na + H2O flecha NaOH + H2
Cual es el volumen de H medido en CN?
Mi pregunta es, ?pero cual hidrogeno tengo que calcular, el hidrogeno de H2O o el H2??? o los dos???
Que lio 🙁
darliens, 12 Años Antes
¡Hola! Pues el hidrógeno que has de calcular es el H2, el de la derecha, porque si te lo piden en condiciones normales, significa que es un gas, y el H2 es un gas a temperatura ambiente, mientras que el agua, H2O, no lo es. De ahí debes deducir que te están pidiendo el H2. Un saludo.
QuimiTube, 12 Años Antes
Muchas gracias!!! hemos metido el problemita de arriba en muchos lados ji ji ji pero ya creo que lo resolvimos… Muchas gracias!
darliens, 12 Años Antes
Me alegro mucho que ya lo tengas resuelto. Ya sabes, si aún te quedan dudas, a preguntar se ha dicho 🙂
QuimiTube, 12 Años Antes
gracias me ayudaron mucho y aprendi mas sobre la quimica
tefyta, 12 Años Antes
Gracias, me alegro mucho, para eso estamos 🙂
QuimiTube, 12 Años Antes
Demonios Xs, ojala fueras mi maestra! explicas sensacional!
Martin, 12 Años Antes
Gracias Martín y bienvenido 🙂 En realidad lo soy, pero virtual jeje
QuimiTube, 12 Años Antes
Excelente explicación.
Jhan carlo, 11 Años Antes
¡Gracias! 🙂
QuimiTube, 11 Años Antes
¡Hola!
De verdad te quiero felicitar por tus excelentes videos, me han servido de mucho, y ahora continuaré con la teoría de bandas, gracias por tu aportación a mi estudio (:
Juany Nava, 11 Años Antes
¡Hola Juany! Muchas gracias a ti por este comentario que nos anima a seguir con el proyecto. Ánimo con tu estudio, un saludo grande.
QuimiTube, 11 Años Antes
Hola, yo tenia una duda sobre estas preguntas. Si me las podrias responder para sacarme las dudas te lo agradeceria un monton.
1) Como estan compuestas las sustancias metalicas segun el modelo del mar de electrones?Por que creen que este tipo de union se da en metales y no en elementos no metalicos?
Franco, 11 Años Antes
¡Hola! Bueno, esto es lo que explicamos en el vídeo… Están compuestas por un «núcleo» donde están juntos todos los cationes del metal correspondiente, y los electrones de valencia de todos estos átomos de metal están en movimiento constante por la totalidad de la red de cationes (de ahí que tengan elevada conductividad eléctrica). Son los metales los que forman este tipo de enlace porque son los que presentan menor energía de ionización y les resulta más sencillo (requieren menos energía, aunque sí que requieren) perder sus electrones de valencia que a los no metales.
QuimiTube, 11 Años Antes
lo siento no escribí bien ., pueden decirme si es lo mismo el mar de electrones y el gas electrónico?
Beatriz Bravo GPO.102, 11 Años Antes
¡Hola! Sí, es lo mismo. Un saludo.
QuimiTube, 11 Años Antes
Hola! Gracias otra vez por tus vídeos y una pregunta… ¿Tienes vídeos sobre formulación?
Me estoy preparando la selectividad para Andalucía por libre y cada vez tengo más lío sobre los prefijos numerales al nombrar. En algunas páginas me dicen que no hay que ponerlos a menos que el elemento tenga varias valencias… en otras aparece el prefijo aunque solo tenga una… por ejemplo, el AlH3 me lo dan por malo como Trihidruro de aluminio en algunas páginas y en otras no…
Estoy hecha un lío y no sé de quién fiarme… He buscado en la página de la IUPAC y todo¿Podrías ayudarme? 🙁
Rocío, 11 Años Antes
Buenas, me pongo en contacto con usted para comentarle si podria grabar o si tuvieras unos apuntes sobre la materia y sus transformaciones (estequiometria , disoluciones…). Esque me stoy preparando para selectividad Andalucía y ese tema mi profesor no lo dio y tengo dudas.
Muchas gracias.
Adrián, 11 Años Antes
Hola Adrián, todavía no tenemos nada sobre estequiometría salvo los cálculos realizados al final de algunos ejercicios (por ejemplo, en los ejercicios de redox suele haber bastante estequiometría posterior, como en este de selectividad de Madrid que te puede servir: http://www.quimitube.com/videos/ejercicio-selectividad-pau-junio-2013-madrid-reaccion-redox-sulfuro-cobre-acido-nitrico/
Especialmente te servirán los apartados c y d.
Espero que podamos grabar pronto estos contenidos.
Un saludo.
QuimiTube, 11 Años Antes
hola, tengo unas dudas sobre maleabilidad, quisiera que me respondieran esta pregunta que me vino en mi examen estaria muy agradecido porfa :).
– la menor maleabilidad del sodio con respecto al magnesio justificando con la teoria del mar de electrones.
diego, 10 Años Antes
¡Hola! Fíjate que la diferencia principal es que el Na pierde 1 electrón (cada átomo) de la capa de valencia, mientras que el Mg pierde 2. Así, el núcleo del Mg estará formado por cationes Mg2+ y ahí estará la clave de la maleabilidad de ambos. Un saludo.
QuimiTube, 10 Años Antes
Hoolaa:) tengo en dos dias la recuperacion de la parte de quimica y tengo un ejercico que no consigo resolver.
Es una tabla en la que te ponen ciertos nombres y te piden tipos de enlace,si hay electrones deslocalizados,si hay iones,si forman moleculas,el estado de agregacion a 20Cº y en que coindiciones es el conductor.Algunas de las columnas ya las tengo echas otras no,pero si me respones a todas mejor para aclarar dudas.
Los nombres son:
1.Sodio
2.Bromo y Calcio
3.Cloro
4.Carbono oxigeno
5.Oxigeno
6.Azufre y Oxigeno
7.Hierro
8.Cobre y Fluor.
Necesito la respuesta cuanto antes,gracias de antemano.
Saludos.
Meryy, 10 Años Antes
Hola Meryy, no puedo responderte a todo ello directamente, por cuestión de que no tengo tiempo material y también porque la idea es que veas los vídeos e intentes responderlo por ti misma (me indicas que tienes hechas algunas pero no cuáles). Piensa que por ejemplo sodio, calcio, hierro y cobre son metales, sus propiedades serán:
http://www.quimitube.com/videos/propiedades-de-los-compuestos-metalicos
En cuanto a cloro, bromo o flúor son elementos diatómicos covalentes:
http://www.quimitube.com/videos/propiedades-de-las-sustancias-covalentes-moleculares
Un saludo
QuimiTube, 10 Años Antes
Hola, te escribo desde México. Estoy viendo tus videos para reaprender química (estoy cursando una segunda carrera y no recordaba nada desde bachillerato) y me están resultando el complemento perfecto para mi curso. Muchísimas gracias por subirlo. Y como a otros, también me gustarían de estequiometria y química orgánica Explicas muy bien. Gracias
Dulce, 10 Años Antes
Hola Dulce:
Muchas gracias por tu comentario, me alegra que te sirva. Espero que durante este otoño pueda subir más material: cinética química, química orgánica y estequiometría. Ya estamos trabajando en ello. Un abrazo y ánimo con tu segunda carrera.
QuimiTube, 10 Años Antes
Hola, para mi tarea de química me poden que represente el tipo de enlace químico desarrollado entre Br e H. Como ya sabemos, ambos tienen un solo electrón en su última órbita y no se cómo se realiza el llamado enlace metálico con la estructura de Lewis para este caso, en el que ambos necesitan perder o ceder ese electrón. Muchísimas gracias.
Catalina, 10 Años Antes
¡Hola! El enlace entre Br y H es covalente porque la diferencia de electronegatividad entre ellos es pequeña, no se trata de un enlace metálico. Te sugiero que veas este vídeo para aclararlo mejor:
http://www.quimitube.com/videos/enlace-covalente-regla-del-octeto-y-estructuras-de-lewis
QuimiTube, 10 Años Antes
Hola disculpa me podrian ayudar con mi tarea de quimica. I de preparatoria
dice que tengo que explicar ¿porque los metales son maleables ? Como punto de partida del mar electronico.
y no se que hacer:( ayuda!
Vanessa, 10 Años Antes
Hola Vanessa, te sugiero que veas el vídeo, este mismo en el que comentas, en el que se explican las características y propiedades de los metales en base a dicha teoría. Un metal es maleable porque las capas que forman el núcleo central pueden deslizarse unas sobre otras, pero lo verás mejor en el vídeo, como te digo. Un saludo.
QuimiTube, 10 Años Antes
Hola tenia una pregunta ; coomo utilizo la teria de enlace metalico
(gas electrónico/mar de electrones/nube de electro) para deducir la estructura de dicho metal ¿?
Espero tener pronto respuestas , que tengo mañana examen.
Un beso desde Bilbao
Naixara M., 10 Años Antes
Hola de nuevo, Naixara, siento como te decía antes no haber podido responder antes, ahora leo que tenías examen. ¡Espero que te vaya bien! Esta pregunta no la he entendido bien, ¿te refieres a la estructura cristalina, por ejemplo hexagonal compacta? Bueno, ya me comentas. Un saludo hasta Bilbao.
QuimiTube, 10 Años Antes
Hola tengo otra pregunta ; como se hace la polaridad de la molecula ¿?
espero tener respuesta pronto
Naixara M., 10 Años Antes
Hola Naixara, respondemos cuando nos es posible, como comprenderás no nos es posible responder inmediatamente. La información que buscas está en la web, puedes buscarla y tardas menos en saber la respuesta. Aquí está el enlace:
http://www.quimitube.com/videos/enlace-covalente-polaridad-de-enlace-y-polaridad-molecular
QuimiTube, 10 Años Antes
Muchas gracias por su respuesta me ha servido de gran ayuda …ojala la proxima vez llegue a tiempo para el examen a pesar de todo me sirve para proximos examenes asi que muchas gracias
un saludo desde Bilbo
y espero que estemos en contacto pronto
🙂
naixara, 10 Años Antes
¡Hola de nuevo! Siento que no llegara a tiempo la respuesta, si intentas preguntarme con algo más de antelación seguro que podré responderte. Un saludo y suerte con tus estudios.
QuimiTube, 10 Años Antes
Como se nombra a un enlace metàlico?
Soli, 10 Años Antes
¡Hola! Bueno, un enlace metálico no tiene en sí mismo nomenclatura, si tienes por ejemplo Na(s) puedes decir simplemente «sodio» o «sodio metálico».
QuimiTube, 10 Años Antes
hola por que los elementos (Ru, Rh, Pd, Os, Ir, Pt, Au se encuentran en su forma libre o nativa en la naturaleza (metales nobles)????
y que tipo de enlace esta presente en esta forma libre???
porfavor me complica esta pregunta
sofi, 9 Años Antes
Hola Sofi, son elementos que no tienen tendencia a formar enlaces en compuestos iónicos (difícilmente oxidables) y que permanecen estables en forma metálica. El enlace que presentarán es enlace metálico, se trata de los átomos del metal unidos entre sí tal y como explicamos en el vídeo.
QuimiTube, 9 Años Antes
Uff, de veras me ayudo… ahora si estoy lista para el concurso!!
Nivedha, 9 Años Antes
¡Mucha suerte!
QuimiTube, 9 Años Antes